Pristatytas naujas būdas formuoti trimačius mikroporėtus darinius. Tokie objektai gali būti taikomi kaip karkasai ląstelių auginimui ir audinių inžinerijai, mikrofluidikoje ir mikromechanikoje. Šis metodas paremtas terminės ekstruzijos 3D spausdinimu ir lazeriniu mikroapdirbimu – šių abiejų technologijų jungimas leidžia greitai ir pigiai gaminti porėtus mikrodarinius, lanksčiai keisti jų geometriją, fizikinius, cheminius, biologinius parametrus. Dabar ši unikali technologija įdiegta ir veikia Vilniaus universiteto Lazerinių tyrimų centre, o Biochemijos institute tiriamos galimybės šiuos gaminius pritaikyti audinių inžinerijai. Tai Lietuvos lazerių, biochemijos ir medicinos sričių mokslininkų bendradarbiavimo rezultatas.
3D spausdinimo pritaikymas audinių inžinerijoje
Naudojant terminės ekstruzijos 3D spausdintuvą (ang. FFF – fused filament fabrication arba FDL – fused deposition modeling) išliejamas norimos geometrijos trimatis darinys (1 pav.). Šiuo atveju tai – darinys, turintis ne tik išorinę geometriją, bet ir vidinę mikroarchitektūrą. Tai pasiekiama tiksliai derinant lydomos medžiagos temperatūrą, padavimo srautą ir trajektoriją. Taip suformuojami dariniai, kurių erdviniai elementai gali būti šimtų mikrometrų, o juos skiriančios poros – dešimčių kubinių mikrometrų dydžio. Taigi taip galima kurti darinius, kurių porėtumas (oro ir viso darinio tūrio santykis) svyruoja nuo 20 iki 60 proc. Porų matmenys gana artimi žinduolių ląstelių dydžiams, tad tokie objektai yra tinkami kamieninių ląstelių auginimui, jų migracijos ir diferenciacijos tyrimui. Gauti rezultatai leidžia teigti, kad visa tai gali būti panaudojama audinių inžinerijoje, pavyzdžiui, pacientui šalinant kaulo defektą. Svarbu paminėti ir tai, kad šiuose darbuose buvo naudojama polilaktinė rūgštis (ang. PLA – polylactic acid), gaunama iš kukurūzų ar cukrašvendrių krakmolo. Ji yra biosutaikoma ir bioskaidi, tad iš jos galima gaminti implantus, kurie laikui bėgant organizme būtų rezorbuojami ir nepaliktų jokių žymių.
Gautų darinių modifikavimas lazeriu
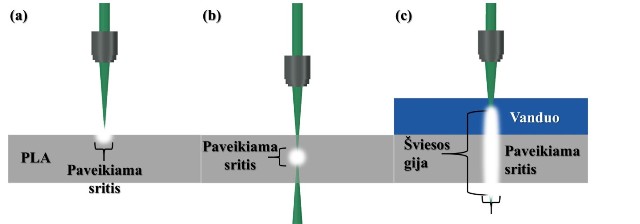
3D darinius galima sėkmingai papildomai modifikuoti Lietuvoje gaminamu ultratrumpųjų impulsų lazeriu „Pharos“ (MGF „Šviesos konversija“). Tam naudojamas efektyvus paviršiaus ir tūrio mikroapdirbimas šviesos gija. Tai nauja lazerinio formavimo kryptis, leidžianti paveikti tiek skaidrias, tiek neskaidrias terpes, jas graviruoti, gręžti, sulydyti ar tiesiog išpjauti įvairias formas. Standartiškai lazeriniame mikroapdirbime naudojamas aštriai fokusuotas pluoštas, o ultratrumpieji impulsai leidžia tiksliai paveikti norimą paviršiaus ar tūrio sritį (2 pav. a ir b). Užliejus bandinį vandeniu (2 pav. c), galima jame indukuoti šviesos giją (filamentą), kuri būtų vienodo šviesos intensyvumo (energijos tankio) išilgai pluošto sklidimo krypties. Tai leidžia tiksliai ir tolygiai naudoti šviesos energiją gręžiant skyles ar pjaustant sudėtingos geometrijos darinius.
Darinių mikrosandarai tirti naudojamas skenavimo elektronų mikroskopas (SEM), didinantis iki 10 tūkstančių kartų ir leidžiantis pamatyti net nanometrų dydžio detales (3 pav.). 4–6 pav. pateikti 3D spausdintuvu pagamintų PLA darinių, apdirbtų lazeriu naudojant šviesos giją, SEM vaizdai, 7 pav. – kaip tokie dariniai matomi plika akimi.
Acetono poveikis
Pastebėta, kad PLA bandinius užmerkus į acetoną jų paviršius smarkiai paveikiamas – formuojasi nanošiurkštus sluoksnis, kuris vėliau virsta į mikrogranules ir delaminuojasi (atsilupa).
Tad vien tik acetono vonelėje galima modifikuoti paviršių taip, kad jis taptų smarkiai hidrofiliškas (vilgus). Ant tokio paviršiaus lašelis vandens nenuteka kaip nuo žąsies plunksnų, bet išplinta, drėkindamas didelį plotą. Šis reiškinys labai svarbus ląstelių adhezijai (prilipimui), nes medžiagos vilgumą lemia ne jos savybės, bet paviršiaus struktūra. Taip nanostruktūrizuojant paviršių galima kontroliuoti hidrofiliškumą, pasiekti reikiamą lygmenį konkrečių ląstelių auginimui.
Organizme ląsteles supa aplinka, kuri iš esmės lemia jų likimą. Nuo šios aplinkos fizinės struktūros ir cheminės sudėties, sąveikų tarp pačių ląstelių ir su tarpląsteliniu užpildu priklauso ląstelių gyvybingumas, dauginimosi intensyvumas bei diferenciacija (specializacija). Gauti rezultatai rodo, kad aptartos PLA struktūros kaip karkasai ląstelių auginimui gerai imituoja užląstelinę aplinką ir yra tinkamas darinys dirbtinių audinių formavimui. Auginant ne visai diferencijuotas (kamienines) ląsteles ant tokių karkasų gaunamas gyvas 3D struktūros dirbtinis audinys, kuris gali būti panaudojamas medicinoje. Derinant 3D spausdintuvu pagamintų karkasų porėtumą su mikrostruktūrizavimu lazerinėmis bei kitomis technologijomis galima valdyti ne tik ląstelių auginimą, bet ir jų diferenciaciją. Apie tai, kad ląstelių prisitvirtinimo paviršiaus subtilios mikrostruktūros yra svarbios jų išsidėstymui ir diferenciacijai, galima spręsti iš 9 pav., kuriame matomos ant 3D suformuotų skirtingo porėtumo struktūrų (a, b, d, e) augančios triušio skersaruožio raumens kilmės kamieninės ląstelės. Ant briaunų išsitempusios ląstelės demonstruoja paviršiaus įtaką jų diferenciacijai. Mikrostruktūrizavimas yra svarbus ir ląstelių adhezijai: daugiau sąlyčio taškų, didesnė tikimybė ląstelei prilipti, o per prisitvirtinimo taškus perduodama informacija daro įtaką ląstelių dauginimuisi, diferenciacijai, jų išgyvenimui arba žuvimui. Skirtingoms ląstelėms reikalingas skirtingas paviršius, kuris nevienodai veikia auginamas ląsteles. Taip, keičiant karkaso struktūrą, galima gauti norimą ląstelių aplinką ir kontroliuoti dirbtinio audinio ląstelių likimą.
Tokie keliomis formavimo technologijomis pagaminti dariniai išsiskiria derinamomis savybėmis makro- ir mikrolygmenyje. Kaip matyti pateiktose mikronuotraukose, objektų forma matoma plika akimi, ji apčiuopiama pirštais (7 pav.), tačiau jie turi vidinę mikrostruktūrą (3–5 pav.) ir yra derinamo paviršiaus šiurkštumo nanometriniame lygmenyje. Tokiems dariniams apibūdinti nebeužtenka žodžio mikroskopiniai. Reikia naujo termino mezoskopiniai. Jis reiškia, kad jų matmenys yra centimetrų dydžio, o funkcines savybes lemia mikrometrinės ar net nanometrinės morfologijos.
Ateities perspektyvos
Ateityje ketinama tokius darinius panaudoti kuriant biorezorbuojamus implantus, kurie galėtų pakeisti dabar naudojamus biologinės kilmės (kito gyvūno) ar sintetinius (biologiškai intertiškus, liekančius organizme visam gyvenimui). Manoma, kad tokie karkasai pagelbėtų protezuojant kaulo defektus ar net chirurgiškai gydant išvaržą. Vilčių suteikia neformalus Vilniaus universiteto tarpdisciplininis mokslininkų kolektyvas, kurio darbo rezultatais ir galimu jų panaudojimu suinteresuota ne viena komercinė bendrovė. Džiugina ir tai, kad tokie moksliniu požiūriu ir pasauliniu mastu unikalūs tyrimai atliekami Lietuvoje.
Daugiau apie tai galima paskaityti šiame moksliniame straipsnyje (anglų k.).
M. Malinauskas, S. Rekštytė, L. Lukoševičius, S. Butkus, E. Balčiūnas, M. Pečiukaitytė, D. Baltriukienė, V. Bukelskienė, A. Butkevičius, P. Kucevičius, V. Rutkūnas, S. Juodkazis, „3D Microporous Scaffolds Manufactured via Combination of Fused Filament Fabrication and Direct Laser Writing Ablation“, Micromachines, 839–858 (2014).



























Komentarų: 4
2014-10-01 18:22
EligijusDaugiau tokių straipsnių.
2014-10-01 22:13
MangirdasEligijau,
Pagal pajegumus, bet, manau, kad po toki ar panasaus lygio straipsni nuo savo laboratorijos galesime kasmet:)
Aciu uz demesi!;)
2014-10-02 16:01
MangirdasJei kam idomu – angliska versija cia:
http://3dprint.com/17403/3d-print-scaffolds-tissue/
2016-01-16 17:34
Evaldas LiutkevičiusPuikus darbas, visus sveikinu !